癌症的攻克一直是人类医学的一大目标,其从人类发现癌症到现在一直在不断的发展。从最传统的放化疗、外科切除到如今火爆的免疫疗法,科学家们始终在探寻是否有方法能够安全有效的解决癌症。之前已经发现酶疗法能够在体内进行催化反应实现肿瘤治疗,并且还能够激活人体免疫能力,增强免疫系统功能。不过天然酶存在成本高、稳定性差、产量低、保存困难和半衰期短等缺点,其实际应用受到限制,也是目前酶疗法迟迟没有进展的原因之一,而纳米酶的出现解决了这一问题。纳米酶是具有催化活性和类酶性能的纳米材料。2007年,Fe3O4纳米颗粒被报道具有模拟天然过氧化物酶的活性,此后发现了数百种纳米材料可以模拟过氧化物酶(POD)、氧化酶(OXD)、过氧化氢酶(CAT)等酶的活性。近日,科学家在纳米酶领域取得了新进展,可以有效用于癌症治疗,引发全身抗肿瘤反应,其论文发表在Science上,标题为Amelioration of systemic antitumor immune responses in cocktail therapy by immunomodulatory nanozymes。科学家设计了一种纳米酶Cu@Fe2C@mSiO2-R848-ICG-AS1411,通过测试其在乳腺癌与黑色素瘤两种小鼠的体内反应。实验发现Cu@Fe2C@mSiO2 NSs和808 nm激光联合使用可以对癌细胞产生强烈的应激反应,导致其体内活性氧(ROS)出现上调,尤其是小鼠中肿瘤部位的ROS生成明显增加。
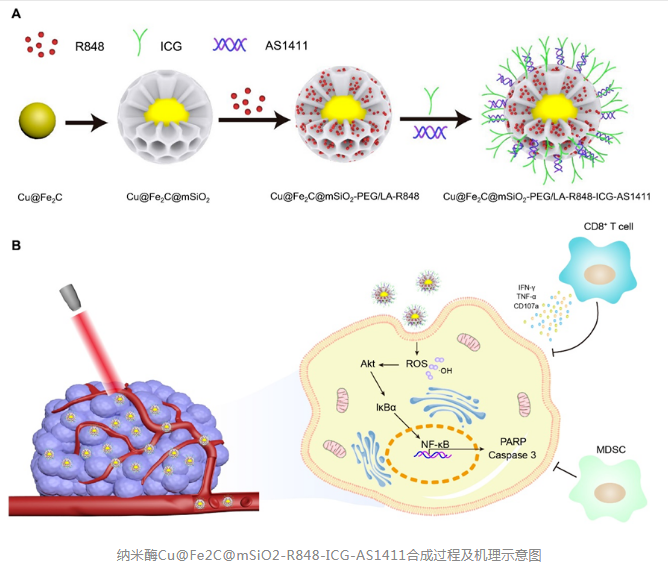
而ROS是一类含有孤电子、化学性质活跃的含氧原子或原子团,包括超氧阴离子(O2−)、H2O2、单线态氧(1O2)、羟基自由基(∙OH)、烷过氧化自由基和脂过氧化自由基等。ROS能够通过介导DNA、蛋白质等化学物质损伤,进而杀伤肿瘤细胞。
ROS之间的平衡可能导致肿瘤细胞死亡。对于纳米酶,可以通过OXD和POD活性产生ROS来诱导氧化应激杀伤肿瘤细胞,也可以通过CAT活性中肿瘤微环境中催化H2O2分解产生O2,缓解肿瘤组织缺氧,间接诱导肿瘤细胞死亡。
在早期肿瘤抑制评估中,在联合激光照射对皮下肿瘤细胞表现出满意的抑制效果,肿瘤几乎消失。纳米酶在808 nm激光照射下对晚期肿瘤也显示出不完全的抑制作用。发现此纳米酶诱导的协同治疗(PTT/CDT/免疫治疗)具有高效的抗肿瘤作用。
此外为了探讨纳米酶系统对小鼠的免疫调节作用,进行了全面和系统的评估。总脾细胞、CD45淋巴细胞和CD8 T细胞的数量和比例的增加证明了纳米酶的固有免疫原性。经过对照试验发现,纳米酶除了免疫原性外,还可以适当提高CD8 T细胞的激活和功能,并减少抑制性细胞(MDSCs)的数量,因为肿瘤部位积累了更多的纳米酶,更容易改善免疫反应。有力地证实了纳米酶系统对癌症的多方面免疫反应调节。
在治疗过程中,还评估了这些纳米酶的体内生物安全性。对这六组小鼠的体重以及关键组织(心、肝、脾、肺和肾)的形态没有影响,表明其具有良好的生物相容性。
纳米酶作为一种新型的抗癌药物,其特点可以模拟天然酶的作用,改变人体微环境,促发免疫反应,应用于抗癌治疗。相对于天然酶,纳米酶表现出以下优势:(1) 高稳定性,具有稳定的纳米结构能够在生理或体内条件下完成催化反应;(2) 多催化活性,同一种纳米酶可以同时具有多种模拟酶活性;(3) 可修饰性,纳米酶可以通过表面修饰增加其靶向性;(4) 制备简单,易于保存,相对于天然酶成本更低等。
不过现阶段还未有一款纳米酶药物问世,说明其临床应用前还存在相关挑战。不过已经有越来越多的研究者开始着手纳米酶,随着后续不断地深入,相信在不久的将来,纳米酶将会从实验室走向临床,做成抗肿瘤药物产物,真正应用于人类肿瘤治疗。
参考资料:
1.https://www.science.org/doi/10.1126/sciadv.abn3883
2.http://www.dxhx.pku.edu.cn/article/2022/1000-8438/20220305.shtml
3.SiegelR. ; Miller K. ; Fuchs H. ; Jemal A. CA Cancer J. Clin. 2021, 71, 7.
DOI:10.3322/caac.21654
4.McNuttM. Science 2013, 342, 1417.
DOI:10.1126/science.1249481