RS构型判断是有机化学的一个基础知识点,是用来表述手性中心碳原子立体构型的一种方法,含有手性中心的化合物在命名时需要标出手性中心的绝对构型,但是很多同学对于RS构型的判断却十分头疼,快来看看你失误在哪里了吧。
1. RS构型的判断基本法则
(1)按次序规则给手性碳相连的各基团排列大小
从第一条来看,次序规则是RS构型判断的基础,如果次序规则都不会判断,那你怎么来判断各基团的大小呢?
(2)将最小的基团放在离眼睛最远的地方。
从第二条来看,将最小的基团放在离眼睛最远的地方,看起来很简单,但是如果你立体化学没有学好,没有立体感,看不懂一个化合物的立体结构式,无法判断各个基团在空间中的相对位置,你又如何能把最小的基团放在离眼睛最远的地方呢?
(3)其它三个基团按由大到小的方向旋转,旋转方向是顺时针的,手性碳为R构型,旋转方向是逆时针的,手性碳为S构型。
第三条与第二条同理,不能看出各个官能团的相对位置,那肯定无法判断顺时针还是逆时针。
下面就让我们来着重地学习一下次序规则和立体化学!

2.次序规则
(1)单原子取代基按原子序数大小排列,原子序数大的顺序在前,原子序数小的顺序在后。同位素中质量高的顺序在前。例如:I>Br>Cl>F>H。

(2)多原子基团比较时,先从第一个原子比起,原子序数大的在前。若第一个原子相同,再比较与第一个原子相连的其它原子,先从最大的比起,仍相同,再比较居中的,最小的,直至比较出谁先大。
例如下面这个化合物:

手性中心与-H、-NH2、-CH2Cl和-CHF2四个基团相连,相连的第一个原子分别是H、N、C、C,其中N原子序数最大,排第1,H原子序数最小,排第4,剩下两个都是碳,没法比较大小,所以要接着往下比,-CH2Cl的碳往下连接的三个原子从大往小排分别为Cl、H、H,-CHF2的碳往下连接的三个原子从大往小排分别为F、F、H,我们要先从最大的原子比起,那么也就是用-CH2Cl的Cl与-CHF2的F相比,Cl比F原子序数大,-CH2Cl比-CHF2次序高。所以-CH2Cl和-CHF2次序分别为2和3。
再例如下面这个化合物:
星标的碳所连的1,2,3三个基团,它们的第一个原子都是碳,所以要接着往下比,我们可以画成树状图:

我们在比较1,2,3时发现,它们都是连一个碳两个氢,接下来再比较最大的碳,碳往下连的过程中,5连的是一个溴,一个氯,一个碳,7连的是一个碳两个氢,8连的是三个氢,那么大小顺序必然是5>7>8,因此三个基团的次序大小为1>2>3。
(3)若参与比较顺序的原子键不到四个,可以补充适量的原子数为零的假想原子。
(4)含有双键或三键的基团,可认为连有两个或三个相同的原子,该原子首次出现时按正常情况处理,重复出现时不再连其它原子。

我们可以看到,乙炔基第一个碳接下来相当于连了三个碳,乙烯基第一个碳接下来相当于连了两个碳,异丙基第一个碳原子接下来也连了两个碳,所以乙炔基肯定最大。接下来比较乙烯基和异丙基,乙烯基中的CH2相当于接下来又连了一个碳,而异丙基中的CH3只连了三个氢,因此乙烯基更大。
再比如拿乙炔基和叔丁基比:虽然第一个碳同样都是连三个碳,但是接下来乙炔基中的CH相当于又接着连了两个碳和一个氢,而叔丁基中的CH3只是连了三个氢,因此乙炔基大于叔丁基。

我们再来比较一下下面两个基团,
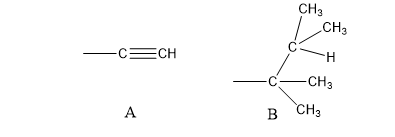
同样是画出它们的树状图:

我们可以看到,A和B第一个碳都是连接三个碳,A中的连的三个碳中最上边的碳相当于又连了两个碳和一个氢,但是前面规则中说过,该原子首次出现时按正常情况处理,重复出现时不再连其它原子,也就是说,括号中的那些碳,相当于没有再连别的原子,而是连个三个原子数为零的假想原子。而B基团中的第一个碳也是连了三个碳,这三个碳中最上边的也是连了两个碳和一个氢,但是这两个碳又分别连了三个氢,所以比A中括号里的碳大。所以B基团比A基团次序大。
(5)构造相同构型不同的手性基团,R优于S。构造相同的烯烃Z优于E。
(6)对于环上有手性的碳原子,相当于连有四个基团,分别是连在环上的两个基团和从手性碳分别往环的两侧延申的两个基团。当延申到环的尽头时,又连回了原来的手性碳,这时相当于连了一个假想的不带取代基的碳原子。
例如下面这个化合物:
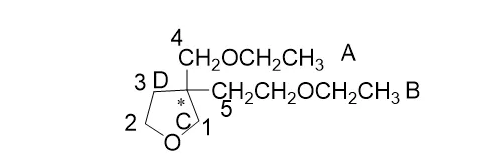
它标星号的手性碳相当于连有四个基团,与环相连的基团A和B分别为 -CH2OCH2CH3和
-CH2CH2OCH2CH3。环上的两个基团一个从C1开始往下延申,标记为C基团,从C1连到O再连到C2再连到C3,当连到C3时,C3再往下连就连回了原来的手性碳,此时不能再往下连了,相当于C3接下来连了一个假想的不连取代基的(C)。因此C基团相当于是:
-CH2OCH2CH2-(C)。同理,从C3开始往下延申,标记为D基团,从C3连到C2连到O连到C1,C1同样又连回了原来的手性碳,相当于C2接下来连了一个假想的不连取代基的(C)。因此D基团相当于是:-CH2CH2OCH2-(C)。所以按照次序规则,环上手性碳连的四个基团大小次序为:C>A>B>D。
3.立体化学
想要判断好绝对构型,学好立体化学是必须的,所以很多同学看完第4讲依然有很多判断绝对构型的题不会做,那是因为你还没学好后面的立体化学,可以先看完7-10讲的立体化学再回来做这里的难题。
比如有些题是让你判断纽曼投影式,费歇尔投影式,伞形式中的手性碳的绝对构型,那么如果你开始立体感不是那么强,不能直接看出来各官能团在空间的相对位置,那么你就要学会将各立体结构式转化成锯架式,因为锯架式的立体感最强,最容易看出各官能团之间的相对位置。
例如:判断下面这个费歇尔投影式手性中心的绝对构型,你可以先转化成锯架式,然后将中间的键轴旋转一下变为第二个锯架式,这样按照箭头的方向从上往下看就可以了。
也可以用我视频里讲的判断RS构型的一个技巧,将小基团位于眼前,其它三个基团按由大到小的方向旋转,旋转方向是顺时针的,手性碳反过来为S构型,旋转方向是逆时针的,手性碳反过来为R构型。这样可以直接用第一个锯架式来按照箭头方向从右往左看。

再比如有些环烷烃手性碳的绝对构型判断,如果你无法直接看出来平面式中各官能团的相对位置,那你就要会把它转化为椅式构象。
例如:判断下面这个化合物手性中心的绝对构型,可以转化成右边的构象式,然后按照箭头方向来看就可以将最小的基团放在离眼睛最远的地方了。
