昨日,根据CDE官网,有三款细胞治疗产品获得临床默示许可,分别是邦耀生物的“靶向CD19非病毒PD1定点整合CAR-T细胞注射液”、广州百吉生物的“BRG01注射液”和重庆精准生物的“C-13-60细胞制剂”。

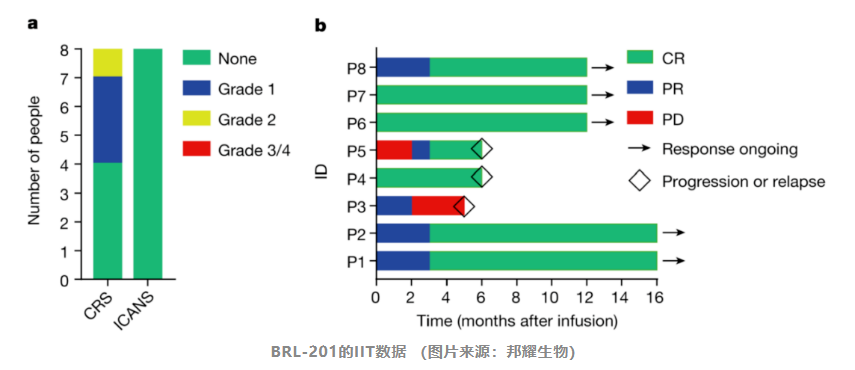
值得注意的是,三款产品中,有两款适应症为实体瘤治疗。根据资料查询,“靶向CD19非病毒PD1定点整合CAR-T细胞注射液”是邦耀生物基于非病毒定点整合CAR-T平台(Quikin CART®)平台开发的产品,研发代号为BRL-201。本次获得临床默示许可的适应症为:复发或难治性 B 细胞非霍奇金淋巴瘤(R/R B-NHL)。BRL-201通过非病毒载体利用CRISPR基因编辑技术实现基因敲除和CAR元件的定点稳定整合,具有PD1基因敲除和CAR均一性稳定表达双重优势。同时利用非病毒载体,还可以避免病毒载体CAR-T的一系列挑战。同时定点整合可以避免随机插入导致的致瘤风险,最大程度保证了CAR-T产品的安全性和有效性。值得一提的是,这是世界首个靶向CD19非病毒PD1定点整合的CAR-T产品。2022年8月31日,BRL-201的IIT数据发表在顶级期刊Nature上,结果显示:完全缓解率(CR)达到87.5%,客观缓解率(ORR)为100%;无癌生存期最长超过2年,且目前仍处于疾病完全缓解的状态。安全性方面,在所有8例患者中,未观察到CAR-T相关的神经毒性和2级以上细胞因子风暴。
百吉生物的“BRG01注射液”是一款通过基因修饰技术将靶向EB病毒(EBV)抗原的受体表达于T细胞表面而制备成的自体T细胞免疫治疗产品,用于治疗复发/转移性鼻咽癌。
EBV感染全球近95%人口,已被世界卫生组织定义为I类致癌物,与其相关的肿瘤主要包括鼻咽癌、EBV阳性的胃癌、淋巴瘤和淋巴细胞增生性疾病等。鼻咽癌是一种发生于鼻咽部黏膜上皮的恶性肿瘤,是常见的头颈部恶性肿瘤之一,其发生发展与EBV的感染密切相关。
BRG01注射液是一款针对鼻咽癌的基因修饰T细胞制品,属于过继性免疫细胞治疗技术,其基本原理是,采集患者血液中的免疫细胞,在体外进行基因工程化改造,增强了T细胞对肿瘤细胞的特异性识别与杀伤效力,这些改造后的细胞回输进患者体内可以达到直接杀伤肿瘤或激发机体免疫功能间接杀伤肿瘤的目的。
精准生物
精准生物的“C-13-60细胞制剂”获得临床试验默示许可,拟开发用于经标准治疗后进展或不耐受,现已无有效治疗手段的晚期末线恶性实体肿瘤。公开资料显示,C-13-60是一款靶向CEA的CAR-T细胞注射液。CEA蛋白通常在癌胚胎的发展过程中表达,在非小细胞肺癌、结直肠癌、乳腺癌等癌细胞表面过度表达。值得注意的是,除低表达于肠上皮细胞外,CEA几乎不在其他正常细胞中表达。C-13-60基于精准生物的RESCAR和PHICAR技术平台开发,能够促进CAR细胞向肿瘤部位聚集,克服肿瘤抑制免疫微环境以提高疗效,同时增强了在肿瘤环境中存活。临床前小鼠体内研究结果显示,C-13-60具有积极的有效性。从今年的CDE审批情况来看,随着中国生物技术的发展,越来越多的公司和产品向CDE提交细胞和基因治疗的临床试验申请,技术路线也是多样开花。