CAR-T细胞治疗作为一种治疗肿瘤的新型精准靶向疗法,在临床肿瘤治疗上表现优异,它能够实现精准、快速、高效的治疗效果,且有可能治愈癌症。
尤其是以CD7 为靶点的CAR-T,因为其HLA(白细胞抗原)与以CD7为靶点的供体源性CAR-T能够相匹配,用以治疗T细胞急性淋巴细胞白血病(T-ALL)患者表现出惊人的效果。
例如最近在成人中,在接受治疗的20例T-ALL患者中,有18例获得了令人印象深刻的完全缓解(CR)。然而,使用HLA匹配的供体来源细胞,仍有一个重大的实际挑战,因为它需要从健康的HLA匹配人群中快速收集T细胞,以进行个性化的产品制造。由于T-ALL的性质和与生产个性化自体产品相关的技术限制,制作耗时长,工作量繁重,价格昂贵等缺点,使用同种异体抗CD7 CART将是一种理想的潜在治疗选择。
同种异体CAR-T细胞是使用同种异体来源或是从诱导性多能干细胞(IPSC)来源的T细胞制备而成的CAR-T细胞,又被称为“现货”(off-the-shelf)和通用型。通常情况下,是从健康的捐赠者体内收集T细胞或直接使用干细胞来源的T细胞,然后经过基因工程敲除/不敲除引起免疫排斥的基因以及装载CAR。
大多数同种异体CAR-T都是需要使用基因编辑技术创建的,但其中的许多技术例如CRISPR-Cas9会诱导DNA双链断裂(DSBs),导致意外的靶向编辑结果,并可能在临床上产生不可预见的后果。
但是科学家发现了一种新的基因编辑器,胞嘧啶碱基编辑器(Cytosine base editors,CBE)。其与CRISPR-Cas9相比,在无需创建DSB的情况下沉默基因表达的效率在90-99%之间,大大减少或消除了多重编辑后不需要的编辑结果。
这项研究结果近期发表在Blood期刊上,论文标题为“Cytosine Base Editing Enables Quadruple-Edited Allogeneic CAR-T Cells for T-ALL”。
科学家用CBE同时进行四个碱基编辑,抑制了CD52、CD7、PD1和TCRα 蛋白的表达,开发出了7CAR8,这是一种靶向CD7的异基因CAR-T。试验证明其与传统CRISPR-Cas9不同,不会影响T细胞增殖,导致异常DNA损伤反应激活或导致多重编辑后的核型异常,大大降低了基因组重新排列或易位的风险。
实验中将17只小鼠随机分为治疗组,并在第11天以三种不同剂量水平(总剂量范围为25倍)给予7CAR8治疗。所有接受7CAR8治疗的小鼠在第35天存活到研究终点,接受最高剂量7CAR8治疗的小鼠在治疗后没有发现疾病。不同实验证实7CAR8在体外和体内细胞系模型以及多种T-ALL的患者衍生异种移植(PDX)模型中具有高度活性。
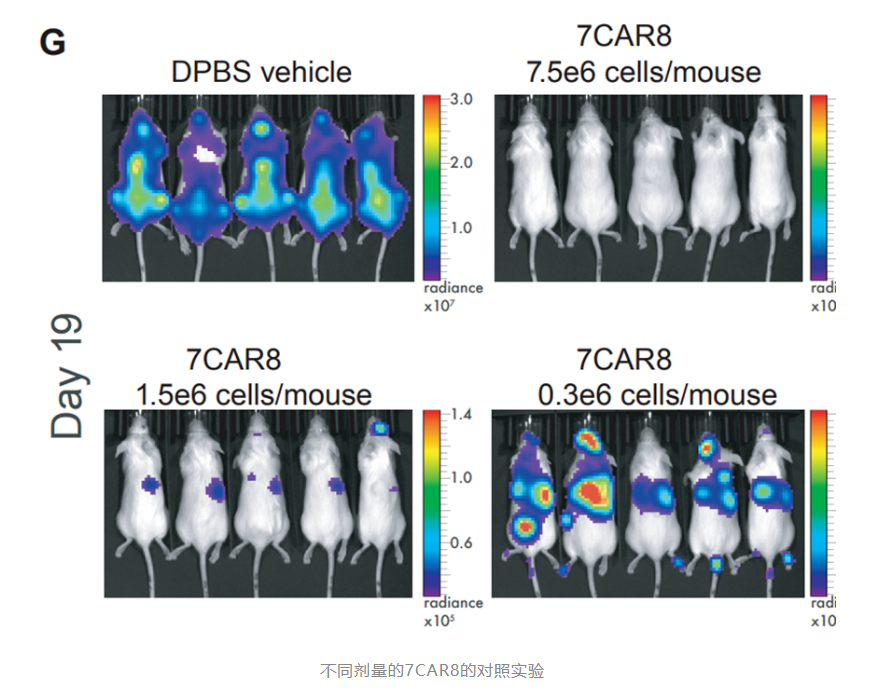
7CAR8对T细胞急性淋巴细胞白血病(T-ALL)非常有效。四倍编辑的7CAR8细胞,具有很高的临床翻译复发和难治性T-ALL的潜力。如果获得批准,有可能成为复发或难治性T-ALL儿童和成人患者的治愈性疗法。它也有可能用于治疗其他CD7+恶性肿瘤,比如T细胞淋巴细胞淋巴瘤,急性骨髓性白血病亚群。
除此之外CBE技术对于需要多重基因编辑的应用来说是一种很有前景的技术,这项研究同样证实了使用CBE进行基因编辑创造同种异体CAR-T的可行性,那么在不同靶向乃至不同领域进行基因编辑也提供了新的思路。
虽然目前多重编辑同种异体的CAR-T细胞具有许多优势,但其还未经过临床的实际考验,其细胞活性、安全性、稳定性还需要时间给出答案。未来如若成功可能市面上会出现更多的不同靶向的同种异体CAR-T,届时不同疾病的患者将拥有更多可选择且有效的治疗方案。
1.Cytosine Base Editing Enables Quadruple-Edited Allogeneic CAR-T Cells for T-ALL | Blood | American Society of Hematology (ashpublications.org)