近日(2022年3月31日),FDA全面暂停了Leronlimab在美的COVID-19临床开发计划,该公司还决定暂停在巴西的COVID-19临床试验,直至独立数据监测委员会分析结果得出。
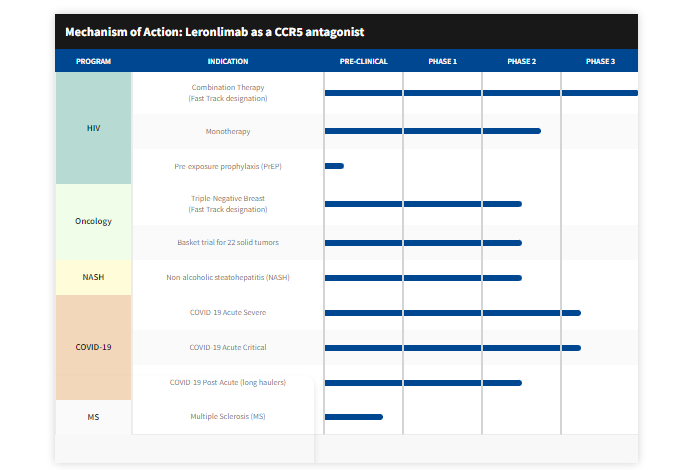
Leronlimab是靶向CCR5的一个人源化IgG4类抗体,为CytoDyn产品线上唯一一款药物。CCR5参与许多病理生理过程,如HIV-1进入CD4+T细胞,促进肿瘤侵袭和转移,非酒精性脂肪性肝炎(NASH)的发病机制和急性移植物抗宿主病(GvHD)的发展等。目前Leronlimab已开展的临床实验的相关适应症涉足HIV感染、GvHD、NASH以及肿瘤等多个疾病领域。除了COVID-19之外,FDA还部分暂停了HIV的临床开发,具体原因,CytoDyn未有披露。
2021年3月5日,CytoDyn发布了leronlimab针对Covid-19危重患者的III 期临床数据,共计招募了394例Covid-19重症患者。数据显示,leronlimab无法改善严重Covid-19患者的存活率。
不过,CytoDyn并未承认这一结果。而是随后就发布了两则声明。第一则申明中,CytoDyn表示leronlimab能够提高一小部分Covid-19患者的存活率,与安慰剂组相比,leronlimab组患者的死亡率降低了24%,加快了出院速度。在后续的声明中,CytoDyn还试图将leronlimab的无效性归咎于其他原因。与安慰剂组相比,65岁以上老年Covid-19患者被随机分配到了leronlimab组,因此该项临床失败。
2021年5月,FDA对公司公开指责,称其歪曲了leronlimab针对COVID-19中的临床数据,主要涵盖两项临床试验CD10( 86名轻度至中度COVID-19患者)和 CD12(394名COVID-19重症患者)。
新冠治疗药物开发方面,舒泰神/InflaRx C5a抗体Vilobelimab治疗新冠重症Ⅲ期宣告了失败。结果显示,Vilobelimab组的死亡率相较于对照组没有达到统计学显著差异。受此消息影响,InflaRx股价当天下跌23%,今日,舒泰神股价同样下跌9.7%。
补体C5激活产生的C5a片段,是炎症信号的放大器,阻断C5a可以阻断其诱导的如中性粒细胞趋化、细胞内溶菌酶的释放、炎性细胞因子水平上升和氧呼吸爆发等生物学功能,抑制炎症级联反应,控制炎症进一步发展。
Vilobelimab为InflaRx公司的针对人C5a分子的单克隆抗体,特异性结合C5a,使C5a丧失结合受体的能力。2015年,舒泰神引进Vilobelimab中国权益。这个临床试验共计入组了209个新冠患者。试验显示,Vilobelimab治疗组28天死亡率略低(31.7% vs 41.6%),但未达到统计学显著。60天的死亡率也未达到统计学显著差异(36.5% VS 47.2%)。
参考出处:
1.https://www.statnews.com/2021/03/07/cytodyns-wild-weekend-of-data-mining-study-results-ends-in-failure-for-its-covid-treatment/2.https://www.biospace.com/article/fda-hits-cytodyn-with-partial-and-full-clinical-holds/3.https://www.statnews.com/2021/03/07/cytodyns-wild-weekend-of-data-mining-study-results-ends-in-failure-for-its-covid-treatment/
4.医药笔记:C5a抗体新冠重症三期临床失败:InflaRx、舒泰神股价齐跌